Bacterias de alta resistencia a los antibióticos, la llamada a la búsqueda de soluciones en I+D de la OMS
Actualmente la resistencia a antibióticos ha provocado que las autoridades sanitarias hagan una llamada a la I+D. Es necesario responder a una de las amenazas más preocupantes para la salud pública mundial de la actualidad. Al menos eso es lo que ha declarado recientemente la Organización Mundial de la Salud (OMS). En este informe, la OMS recoge lista de las bacterias para las que, debido a su resistencia a los antibióticos existentes, se necesitan nuevas soluciones.
Las bacterias generan, por mutaciones espontáneas, resistencia a los antibióticos al poco de ser descubiertos. Por ejemplo, sólo 5 años después del descubrimiento de la penicilina se empezaron a detectar bacterias resistentes a ella. Enfermedades como la tuberculosis o la neumonía son cada día más difíciles de tratar debido al aumento de la resistencia de estas bacterias a los antibióticos utilizados para tratarlas.
El informe de la OMS pone de relieve especialmente la amenaza sanitaria de alta gravedad que suponen las bacterias que ya son resistentes los antibióticos conocidos. Cada vez es más urgente encontrar una solución para poder luchar contra la resistencia a los antibióticos o de lo contrario, enfermedades que se curaban de una manera sencilla pasaran a ser causa de mortandad. De hecho, el gobierno británico ha informado que se espera que en 30 años las bacterias resistentes a los antibióticos maten a más gente que el cáncer.
Bacteriófagos, ¿una alternativa a los antibióticos?
Los bacteriófagos, también llamados fagos, son virus que infectan a las bacterias y parasitan su maquinara enzimática. Hoy en día, el uso de los bacteriófagos se está postulando como la alternativa potencial para hacer frente al problema de la resistencia a los antibióticos.
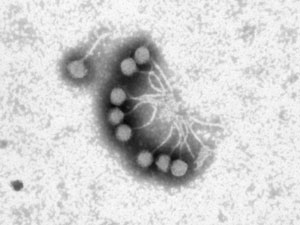
Fuente: Universidad de Barcelona. Dra. Muniesa
Los bacteriófagos son capaces de matar las principales bacterias responsables de diversas patologías. Para conseguirlo se unen a la bacteria patógena huésped, introducen su material genético, se replican dentro de ella y la destruyen produciendo la lisis bacteriana (ruptura de la membrana celular de la bacteria). De esta manera a partir de un fago se generan nuevas generaciones de virus listas para actuar sobre el resto de las bacterias, produciendo una reacción en cadena que elimina el patógeno.
A diferencia de los antibióticos, los fagos son muy específicos, afectan sólo a la bacteria diana sin dañar ninguna otra célula y además no se han descrito efectos secundarios en su utilización. En cambio, los antibióticos afectan a un amplio número de bacterias, ocasionando problemas con la microbiota intestinal. A este respecto y citando a Michael Schmidt de la Universidad Medica de Carolina del Sur podríamos decir que “los antibióticos son como un gran martillo y necesitamos un misil guiado”.
Los fagos son elementos ubicuos, pueden encontrarse en diferentes lugares en la naturaleza, tanto a elevadas y como a bajas temperaturas, en ambientes áridos, desérticos, acuáticos, ácidos, etc. De hecho, se calcula que es la entidad biológica más abundante en la Tierra.
Durante los años 40, en la antigua Unión Soviética, se empezó a investigar lo que se conoce actualmente como terapia fágica, que es el uso de los bacteriófagos para la eliminación de patógenos en sustitución de los antibióticos.
Como reseñábamos en el artículo Seguridad alimentaria y bacteriófagos: Hacia dónde va la I+D orientada al control de patógenos, implica que en principio no hay razones para considerarlos inseguros o potencialmente peligrosos para la salud. En los últimos años la Agencia Europea de Medicamentos y el Instituto Nacional de la Salud (EUA) han organizado varias jornadas dedicadas al uso terapéutico de bacteriófagos.
En países como Bélgica, Francia y Países Bajos se han hecho estudios para tratar a pacientes quemados con cocktails de bacteriófagos y en algunos estados de EEUU, como Texas, se considera el uso de bacteriófagos como substancias naturales que se pueden usar para complementar las terapias tradicionales.
Fagos para uso veterinario
En el mundo animal también se está empezando a plantear el uso de bacteriófagos. Cada vez hay más restricciones para el uso de antibióticos en la ganadería, debido sobre todo al interés por evitar la resistencia de las bacterias a los antibióticos.
En esta línea, ya existen en el mercado algunos compuestos como Intralytix, una preparación a base de fagos para uso en veterinaria. Esta sustancia es efectiva frente a Salmonella y C. perfringens.
Para profundizar en la aplicación de bacteriófagos para uso veterinario, recomendamos la lectura del artículo: “Bacteriófagos para el control microbiológico de la agricultura”.
No obstante, aún quedan cuestiones que deben ser tenidas en cuenta y la I+D+i trabaja en aumentar el conocimiento sobre los mecanismos de acción de los fagos en su ofensiva contra las bacterias patógenas y, por otro, en la minimización de los riesgos en relación a la resistencia y adaptación de las bacterias a los bacteriófagos y la adaptación de estas entidades biológicas frente a posibles mutaciones de las bacterias diana.
En AINIA estamos trabajando en una línea de I+D orientada a la búsqueda de soluciones de biocontrol basadas en bacteriófagos.
Aislamiento, bioproducción y encapsulación, tres etapas clave para conseguir un producto destinado a “terapia fágica”
El proceso para conseguir un producto destinado a “terápia fágica” se inicia con el aislamiento de los bacteriófagos. Los bacteriófagos se encuentran de forma natural junto con la bacteria que le sirve de huésped. Es por ello que para garantizar el éxito de esta fase es necesario partir de muestras que contengan la bacteria que se quiere eliminar, es decir, la patogénica.
Sea cual sea el sector de aplicación final, siempre se buscará seleccionar un bacteriófago con capacidad lítica, es decir aquellos que, por su naturaleza más virulenta, provocan la lisis de la bacteria huésped en su proceso de multiplicación.
A partir de muestras que contengan la bacteria huésped, se puede trabajar en un aislamiento directo o en un aislamiento con un paso de intensificación previo. El aislamiento implica una siembra en placa en la que en lugar de apreciarse las colonias de bacteria huésped se aprecia ausencia de las mismas o “calvas”.
Una vez aislado el bacteriófago se deben definir las condiciones óptimas para su multiplicación.
De forma general el proceso de multiplicación de los fagos presenta 3 etapas:
- En la primera etapa se produce el crecimiento de la bacteria huésped, generalmente hasta alcanzar su fase exponencial (108 -109 ufc/mL).
- En la segunda se inocula el sistema con un volumen de bacteriófagos crecidos en el mismo medio de cultivo. En el caso de que la bacteria huésped esté en fase logarítmica de crecimiento, los bacteriofagos se multiplican rápidamente, provocando en el proceso la lisis de la bacteria huésped.
- En la tercera etapa se separará la biomasa residual del lisado mediante filtración, separando de esta manera los bacteriófagos de los restos celulares de la bacteria huésped.
La fase final implica la estabilización de los bacteriófagos. El reto en esta etapa radica en conseguir mantener la viabilidad de los lisados obtenidos, ya que el tiempo de vida útil del bacteriófago si no se encuentra con la bacteria huésped es muy limitado. Por ello, se están considerando estrategias de estabilización como el pulse combustion drying o spray drying. Otras estrategias como la liofilización presentan pérdidas de viabilidad mayores.
Nuestros técnicos están estudiando el potencial de los fagos para su aplicación en terapias sustitutivas de antibióticos en el ámbito sanitario, pero también en el agropecuario y agroalimentario. Si está interesado en saber más acerca de este tema y de los proyectos que estamos desarrollando en este ámbito, contacte con nosotros, tenemos una línea de investigación específica en este campo.
Noticia en Pharma Market: enlace.










